A finales de 2020 se descubrió que los incendios que habían devastado Australia un año antes habían provocado una importante destrucción del ozono de la capa de ozono en el hemisferio austral. Ahora, un estudio efectuado por investigadores del Instituto de Tecnología de Massachusetts (MIT) ha identificado el mecanismo por el cual tiene lugar esta alarmante destrucción, toda una advertencia de lo que puede suceder con un planeta sobrecalentado y donde los incendios son cada vez más abundantes, duraderos y masivos.
Además de devorar millones de hectáreas de bosques, los enormes pirocumulonimbos —nombre técnico que reciben las columnas de humo que alcanzan alturas de kilómetros— se elevaron hasta alcanzar la estratosfera, inyectando millones de toneladas de aerosoles. Meses después, los datos registrados por los satélites revelaban que este humo, de alguna manera, había provocado la destrucción de parte de la capa de ozono. En concreto, entre un 3% y un 5% del ozono presente en las latitudes medias del hemisferio sur, en el cinturón localizado sobre Australia, Nueva Zelanda y regiones de África y Sudamérica. Además, tras alcanzar las regiones polares arrastrados por las corrientes de aire estratosféricas, habían provocado la destrucción del ozono de los bordes del agujero de ozono localizado sobre la Antártida, ampliándolo en 2,5 millones de Km2 —un 10% de su extensión total antes de que se diese este evento.
La constatación de los datos recolectados motivó que científicos del MIT comenzasen a investigar el mecanismo por el cual el humo de los incendios había provocado esta masiva destrucción de ozono. Un mecanismo que ahora ha sido identificado gracias a un estudio que ya había anticipado sus primeros resultados hace apenas un año.
Para determinar el proceso destructivo, el primer paso fue reexaminar lo que ya se sabía: cómo se produce la destrucción del ozono en los vértices polares, y más concretamente, sobre el polo sur.
El ejemplo del polo sur
Todo arranca con los compuestos clorofluorocarbonados (los CFCs), prohibidos desde la década de 1990, pero que durante mucho tiempo fueron empleados y emitidos de forma masiva a la atmósfera. Los CFCs son compuestos de elevada persistencia pero, al mismo tiempo, bastante fotorreactivos bajo la acción de la intensa radiación ultravioleta que alcanza las capas altas de la atmósfera. Con el paso del tiempo, estos CFCs se han ido degradando y rompiendo, dando lugar a la formación de otros compuestos clorados, entre los que destaca el ácido clorhídrico (HCl).

Si bien el ácido clorhídrico en estado gaseosos es poco reactivo y, por tanto inocuo, para el ozono, el problema llega cuando algo provoca la ruptura de este HCl, ya que en este estado, sí presenta mucha tendencia a reaccionar con los átomos de oxígeno del ozono (O3). En las regiones polares, la disociación del HCl se produce cuando éste es absorbido por las gotas de ácido nítrico y agua que contienen las nubes estratosféricas. Al absorberse sobre la superficie de estas gotas, se dan las condiciones adecuadas para que el ácido clorhídrico se disuelva y se libere el átomo de cloro.
La presencia de estas nubes se restringe a las latitudes polares, donde se dan las condiciones adecuadas de temperatura y baja humedad para su formación, condiciones que no se dan en latitudes más bajas. Con esta condición, los investigadores volvieron sus ojos a los aerosoles derivados de los incendios para ver si, de alguna manera, estos también desencadenaban una reacción análoga.
La molécula destructora del ozono
La clave en este caso radica en la naturaleza orgánica de las diminutas partículas que integran estos aerosoles. Atendiendo a su origen vegetal, estas partículas contienen ácidos orgánicos capaces de disolver el ácido clorhídrico y debilitar los suficiente el enlace H-Cl para permitir la liberación del átomo de cloro.

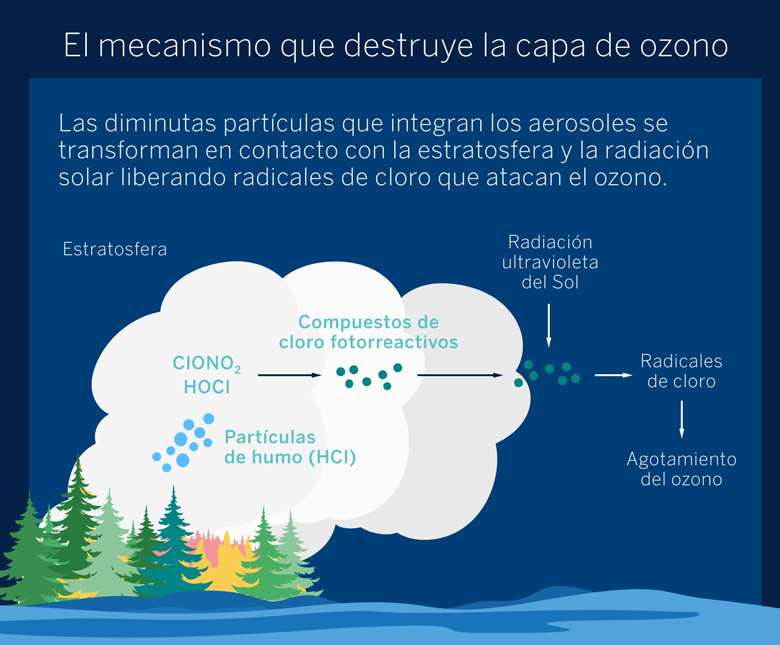
Durante su ascenso, los aerosoles absorben en su superficie moléculas de agua y, al alcanzar la estratosfera, hacen lo propio con el HCl presente. La combinación de agua y ácidos orgánicos genera unas condiciones propicias para que el HCl se disuelva y se debilite lo suficiente el enlace molecular para que el átomo de cloro reaccione con otros compuestos clorados presentes en la estratosfera, y derivados de los CFCs, como el ácido hipocloroso (HClO) y el nitrato de cloro (ClNO3). De esta forma, se originan compuestos fotorreactivos que, bajo la acción de la energética radiación solar UV incidente a esas alturas, se descomponen liberando radicales Cl (átomos de cloro libres con una enorme avidez por reaccionar con otros átomos).

Estos radicales de cloro son, en última instancia, los que atacan al ozono (O3) dando lugar a la formación de oxígeno molecular (O2) y monóxido de cloro (ClO), un compuesto bautizado como la molécula destructora del ozono, debido a su extrema capacidad reactiva. El oxígeno del ClO reacciona enseguida con los átomos de oxígeno libres presentes en la estratosfera para formar O2 y desprenderse en el proceso del radical Cl que, de este modo, vuelve a destruir otra molécula de ozono.
Comentarios sobre esta publicación