—Rutherford, ¡esto es transmutación!
—Por Dios, Soddy, no le llames transmutación. Nos cortarán la cabeza por alquimistas.
Así reaccionaron el físico neozelandés Ernest Rutherford y su discípulo inglés Frederick Soddy ante el sorprendente resultado de una serie de cuidadosos experimentos que realizaron en 1901 en la Universidad McGill de Montreal (Canadá). Llevaban tiempo intentando entender el fenómeno de la radiactividad, descubierto por Becquerel y descrito por Marie y Pierre Curie. Y por fin habían conseguido demostrar que en los materiales radiactivos los átomos se desintegran, de modo que los átomos de un elemento radiactivo se transforman en otro elemento.
Así que la transmutación, que habían buscado durante tantos siglos los alquimistas, ocurría de manera espontánea y natural. La idea era tan rompedora que Rutherford y Soddy evitaron añadirle prejuicios y hablaron de transformación en lugar de transmutación cuando en 1902 publicaron “La causa y naturaleza de la radiactividad”, que condensaba sus experimentos en la teoría de la desintegración atómica. Con ella rompieron el dogma científico de que el átomo era indivisible (que es lo que significa átomo en griego).
Ernest Rutherford (30 agosto 1871 – 19 octubre 1937) nació el mismo año en que Henry Morton Stanley finalmente encontró a otro famoso explorador en medio de África y pronunció una de las más icónicas frases de la historia británica: “Doctor Livingston, Supongo”. Rutherford, nacido en una granja de la remota colonia de Nueva Zelanda, fue enlazando una beca con otra y así llegó a un mítico laboratorio de la Universidad de Cambridge, en Inglaterra, en 1895, el año del descubrimiento de los rayos X. En aquella época, tocaba un descubrimiento revolucionario por año: en 1896 fue la radiactividad y en 1897 el jefe de Rutherford, J.J. Thompson, arrancó del interior del átomo una partícula más pequeña y de carga negativa: el electrón.
Rutherford se subió a esa ola de deslumbrantes descubrimientos y llegó a ser el líder de una nueva generación de exploradores del Imperio Británico que, en lugar de perderse en la inmensidad de un continente, prefirieron buscar dentro de la cosa más pequeña que se conocía: el átomo. Sin brújulas ni mapas, Rutherford logró hacerse una buena idea de cómo es el átomo gracias a la radiactividad.

Primero identificó los tres tipos principales de radiactividad: rayos alfa, rayos beta y rayos gamma. Y siguió estudiando la transmutación. Vio cómo aparecían átomos estables de plomo en medio de un mineral radiactivo de uranio. No había manera de saber cuándo se iba a transformar un átomo en concreto, pero Rutherford se fijó en que cualquier muestra (más grande o más pequeña) de un mismo elemento radiactivo tardaba exactamente el mismo tiempo en quedar reducida a la mitad. Ese tiempo, llamado semivida, convertía a los elementos radiactivos en perfectos cronómetros.
Conociendo esa velocidad constante con la que el uranio se transforma en plomo y midiendo la cantidad de plomo que había en una roca de pechblenda (mineral de uranio), Rutherford y su colega Boltwood calcularon en 1907 que alguna de aquellas piedras tenía al menos 1.000 millones de años: ¡Era muchísimo más vieja de lo que entonces se pensaba que era la Tierra!
Además de entender a fondo la radiactividad, Rutherford le dio su primera utilidad práctica (mucho antes que las aplicaciones médicas, bélicas o energéticas): calcular la edad de la Tierra. Por todo ello recibió el premio Nobel de Química en 1908. Aunque bien podría haber recibido dos Nobel más por sus siguientes descubrimientos:
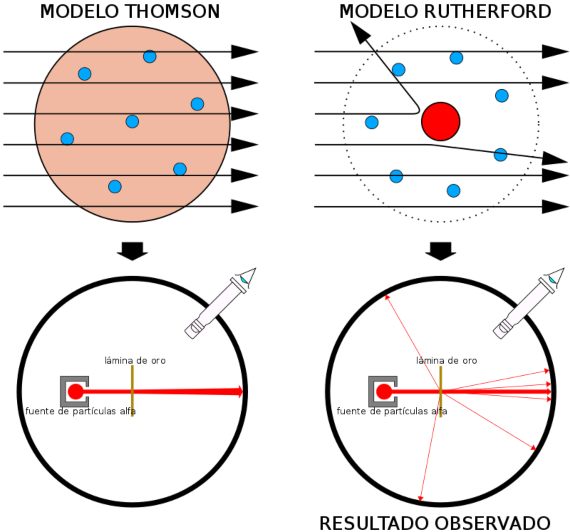
- Primero usó la radiactividad para explorar el interior de los átomos. Junto con su alumno Geiger, el hombre que aprendió a contar la radiactividad, Rutherford disparó rayos alfa contra una finísima lámina de oro y observó atónito cómo alguna de esas partículas alfa (muy pocas, una de cada 20.000) rebotaban hacia atrás. «Fue tan increíble como disparar una bala de cañón contra un papel y ver como rebota y te golpea», afirmó entonces. Recuperado del impacto, en 1911 dedujo que aquello solo era posible si los átomos tenían un núcleo, con carga positiva, que concentraba casi toda su masa en un centro aún mucho más diminuto. Si ampliásemos un átomo hasta el tamaño de un gran estadio de fútbol, el núcleo sería tan pequeño como la moneda que lanza el árbitro. Había nacido el modelo atómico de Rutherford, perfeccionado luego por su alumno Bohr: esa imagen tan familiar del átomo, con los electrones girando alrededor de ese núcleo.
- En su laboratorio él siguió bombardeando átomos con rayos alfa, hasta que en 1919 consiguió transformar átomos de nitrógeno en oxígeno: se convirtió así en “el primer alquimista con éxito de la historia”. Aquella transmutación de nitrógeno en oxígeno fue la primera reacción nuclear artificial; y, entre sus restos, Rutherford encontró el protón, una nueva partícula subatómica con carga positiva.
Aquel fue el punto culminante de la carrera de éxitos de Rutherford como explorador subatómico. Entonces Rutherford se convirtió en el jefe del Laboratorio Cavendish de Cambridge y allí siguió creando escuela: uno de sus discípulos, James Chadwick, consiguió cerrar la trilogía de partículas básicas del átomo, al descubrir el neutrón en 1932. Y en esa época dorada, Chadwick y otros tres miembros más del equipo de Rutherford lograron el premio Nobel.
Mientras tanto, Frederick Soddy (2 de septiembre de 1877 – 22 de septiembre de 1956) había seguido estudiando la desintegración natural de los elementos radiactivos y descubrió en 1913, al mismo tiempo que Kazimierz Fajans, las reglas de la transmutación: cuando un átomo emite espontáneamente una partícula alfa, retrocede dos casillas en la tabla periódica (ej: el uranio–238 se transforma en torio); cuando un átomo emite una partícula beta, avanza una casilla (ej: el carbono–14 se transforma en nitrógeno).

Siguiendo esas reglas, conocidas como la ley de Fajans-Soddy, se producen las cadenas de desintegración naturales, como la que empieza en el radiactivo uranio–238 y termina en el estable plomo, pasando por productos intermedios como el radio o el uranio-234. Y estudiando paso a paso esas cadenas, Soddy descubrió por el camino los isótopos: distintas versiones de un mismo elemento, con átomos que pesan diferente pero que tienen las mismas propiedades químicas.
El Nobel de Química de 1921 reconoció los descubrimientos de Soddy, en los que el escritor H.G. Wells se había inspirado para escribir su novela de ciencia-ficción “La liberación mundial” (1914). Ese libro, que Wells dedicó a Soddy, anticipaba el peligro de las armas nucleares, casi 20 años antes de que Leó Szilárd concibiera la idea de reacción en cadena.
A Soddy le preocupaba mucho el uso que se hacía de los descubrimientos científicos y eso le llevó a escribir en 1926 una crítica radical de la economía occidental, analizándola mediante leyes físicas de la termodinámica. Según Soddy, el sistema confunde la riqueza con la deuda, y también fue pionero criticando el crecimiento económico basado en el uso de combustibles fósiles para obtener energía. Sus propuestas para una reforma del sistema monetario, que hoy son prácticas comunes, fueron entonces despreciadas e ignoradas por excéntricas… como si Soddy fuera un alquimista económico en busca de una piedra filosofal para transformar la deuda en riqueza.
Comentarios sobre esta publicación